Advertisement
Grab your lab coat. Let's get started
Welcome!
Welcome!
Create an account below to get 6 C&EN articles per month, receive newsletters and more - all free.
It seems this is your first time logging in online. Please enter the following information to continue.
As an ACS member you automatically get access to this site. All we need is few more details to create your reading experience.
Not you? Sign in with a different account.
Not you? Sign in with a different account.
ERROR 1
ERROR 1
ERROR 2
ERROR 2
ERROR 2
ERROR 2
ERROR 2
Password and Confirm password must match.
If you have an ACS member number, please enter it here so we can link this account to your membership. (optional)
ERROR 2
ACS values your privacy. By submitting your information, you are gaining access to C&EN and subscribing to our weekly newsletter. We use the information you provide to make your reading experience better, and we will never sell your data to third party members.
Synthesis
Un catalizador de níquel funciona como “engranaje” para producir ácidos grasos.
La reacción catalítica añade dióxido de carbono a determinados enlaces C–H en alcanos y alquenos.
by Stu Borman
May 8, 2017
| A version of this story appeared in
Volume 95, Issue 19
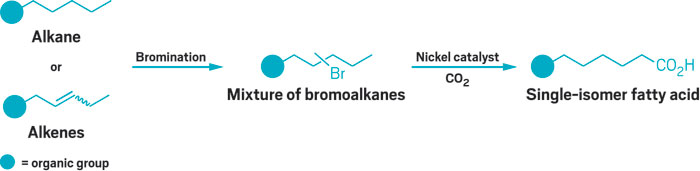

Muchos de los enlaces C-H en hidrocarburos guardan bastante parecido con reactivos químicos, Por lo tanto, los químicos sintéticos a menudo tienen que echar mano de grupos activantes o directores para que las reacciones ocurran en determinados enlaces preferentemente. En esta nueva reacción, un catalizador de níquel se desplaza a lo largo de una cadena hidrocarbonada para activar enlaces C–H específicos sin necesidad de utilizar grupos directores o activantes (Nature 2017, DOI: 10.1038/nature22316).
El método, desarrollado por Rubén Martín del Instituto Catalán de Investigación Química (ICIQ) y colaboradores, proporciona una nueva ruta para la preparación de ácidos grasos, comúnmente utilizados por la industria en la preparación de jabones, detergentes, caucho, plásticos y tintes. Cada reacción produce un único isómero del correspondiente ácido graso al añadir CO2 a un enlace C–H determinado en una mezcla pura de alcanos o alquenos a partir de un derivado muy económico de petróleo.
Actualmente, en los procesos industriales, los ácidos grasos se producen mediante hidrólisis de derivados lipídicos naturales o mediante la hidrocarbonilación de alquenos con monóxido de carbono. Matthew Gaunt y Patrick Williamson, de la Universidad de Cambridge, explican en un comentario que acompaña al nuevo artículo de Nature, que estos procesos requieren separaciones y purificaciones para aislar ácidos grasos determinados. La reacción de Martín evita estos pasos creando regioisómeros específicos, “una increíble proeza en selectividad,” escriben Gaunt y Williamson.
En la reacción, los químicos realizan una bromación en una mezcla de alcanos o alquenos específicos. Cada tipo de hidrocarburo puede tener un grupo funcional orgánico terminal. Las moléculas de alqueno en cada mezcla deben tener la misma longitud de cadena, pero las posiciones de los dobles enlaces pueden variar. El bromo puede ocupar cualquier posición en los alcanos o alquenos, puesto que su localización no afecta a la selectividad en la adición de CO2. Un catalizador de níquel sustituye al bromo y recorre la cadena hasta el enlace C-H seleccionado.
Esta técnica explota la β eliminación de hidruros, una reacción normalmente indeseable, que sucede espontáneamente en reacciones de sustitución en haluros de alquilo. Con cada eliminación, el catalizador se desplaza al carbono contiguo y prosigue su camino, de uno en uno, a lo largo de la cadena hasta llegar al C–H objetivo, donde el CO2 lo sustituye. Esta técnica del “engranaje” ya se había utilizado antes, aunque de formas menos vérsatiles y, por lo general, con catalizadores de metales nobles mucho más caros.
Los investigadores controlan selectivamente la posición mediante la temperatura de reacción. A menor temperatura, el control cinético posiciona el CO2 en el sitio con menor impedimento estérico: alquilo terminal. A mayor temperatura, el control termodinámico determina que el CO2 se localice en posiciones intermedias en la cadena. “Existe un número importante de aspectos remarcables en este trabajo, pero lo más impresionante es el cambio en la selectividad que se modula simplemente mediante la temperatura,” comenta Olivier Baudoin de la Universidad de Basilea, quien recientemente desarrolló otra reacción de “engranaje.”
“El objetivo de poder utilizar fuentes de hidrocarburos sin procesar y convertirlos en reactivos químicos de gran interés resulta fascinante, y en raras ocasiones he visto demostrado su gran potencial de una forma tan completa como este trabajo,” comenta M. Christina White, química sintética de la Universidad de Ilinois, Urbana-Champaign. “Esta reacción va más allá de la validez del concepto y es útil de forma inmediata. La habilidad para explotar una ruta de β eliminación que favorece la funcionalización de un sitio determinado, inspirará sin lugar a dudas el diseno de reacciones en el futuro.”
Traducción al español producida por Irene Maluenda Borderas de Divulgame.org para C&EN. La versión original (en inglés) del artículo está disponible aquí.

Join the conversation
Contact the reporter
Submit a Letter to the Editor for publication
Engage with us on Twitter