Advertisement
Grab your lab coat. Let's get started
Welcome!
Welcome!
Create an account below to get 6 C&EN articles per month, receive newsletters and more - all free.
It seems this is your first time logging in online. Please enter the following information to continue.
As an ACS member you automatically get access to this site. All we need is few more details to create your reading experience.
Not you? Sign in with a different account.
Not you? Sign in with a different account.
ERROR 1
ERROR 1
ERROR 2
ERROR 2
ERROR 2
ERROR 2
ERROR 2
Password and Confirm password must match.
If you have an ACS member number, please enter it here so we can link this account to your membership. (optional)
ERROR 2
ACS values your privacy. By submitting your information, you are gaining access to C&EN and subscribing to our weekly newsletter. We use the information you provide to make your reading experience better, and we will never sell your data to third party members.
Biological Chemistry
Una nueva visión del espliceosoma
Biólogos estructurales capturan un estado importante de la maquinaria celular responsable de que los humanos seamos más complejos que los gusanos.
by Sarah Everts
May 24, 2017
| A version of this story appeared in
Volume 95, Issue 22

Los humanos comparten un número parecido de genes codificantes de proteínas con el gusano Caenorhabditis elegans y sin embargo somos, sin duda, organismos más sofisticados. Esta diferencia de complejidad se debe sin duda al espliceosoma, una pieza de ingeniería bioquímica espectacular que se halla en el núcleo celular.
El espliceosoma corta las secuencias innecesarias (intrones) del RNA después de la transcripción, y luego junta los trozos restantes para formar el RNA mensajero (mRNA). La variabilidad que introduce el espliceosoma al combinar el RNA no-intrónico hace que las células humanas puedan sintetizar diez veces más proteínas de las que codifican nuestros genes.
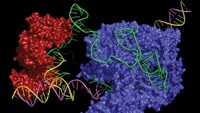
Ahora, gracias a la microscopía crioelectrónica, los investigadores han logrado una visión casi atómica de esta maquinaria celular en un estadio pre-catalítico, justo antes de ‘tomar la decisión de empezar a “cortar” el DNA (Nature, 2017, DOI: 10.1038/nature22799).
Docenas de proteínas y cinco complejos RNA-proteína, llamados ribonucleoproteínas, vienen y van mientras el espliceosoma corta el RNA recién transcrito del DNA, justo antes de que empiece la producción de proteínas. Durante los cortes, se producen siete reordenamientos colosales del espliceosoma que van desde el montaje, pasando por su activación hasta la catálisis.
La presente investigación, llevada a cabo por Clemens Plaschka, Pei-Chun Lin y Kiyoshi Nagai del Laboratorio de Biología Molecular del Consejo de Investigación Médica, ha capturado el espliceosoma en un momento particularmente importante: cuando la máquina ha cargado el RNA sin cortar pero todavía no ha empezado la catálisis, explica Yigong Shi de la Universidad de Tsinghua, que no trabajó en esta investigación. Es un paso de compromiso, un momento de decisión antes de cortar.
El equipo encontró que 24 proteínas asociadas al espliceosoma ayudan a mantener la máquina en un ‘estado precatalítico’. Después, estas 24 proteínas se van y dejan sitio a otras 22, que ayudan al espliceosoma a recolocarse y prepararse para la catálisis, dice Plaschka. El trabajo proporciona “un marco para analizar el mecanismo de activación y determinar el orden de eventos moleculares que llevan a la formación del sitio activo del espliceosoma,” explican los investigadores en el artículo.
A día de hoy, los biólogos estructurales habían podido capturar cuatro estados consecutivos del espliceosoma a resolución atómica, añade Shi. “Esta quinta estructura es un paso importante para la recapitulación del ciclo catalítico completo.”
Traducción al español producida por Fernando Gomollón Bel de Divulgame.org para C&EN. La versión original (en inglés) del artículo está disponible aquí.

Join the conversation
Contact the reporter
Submit a Letter to the Editor for publication
Engage with us on Twitter